https://apph5.cloudgx.cn/article/sync1990252997886541824
弓形虫病是一种复杂的人兽共患病,其病原体弓形虫的繁殖“幕后开关”究竟何在?这一直是长期困扰学界的难题。近期,广西大学科研团队取得研究进展,找到了控制弓形虫快速繁殖的核心机制。
广西大学动物科学技术学院动物寄生虫病防控团队副教授胡丹丹、宋星桔在人兽共患弓形虫病研究中取得新进展,研究成果以“Toxoplasma gondii chromatin remodeler SWI/SNF controls parasite division and gene expression”为题,发表在𝘕𝘢𝘵𝘶𝘳𝘦 𝘊𝘰𝘮𝘮𝘶𝘯𝘪𝘤𝘢𝘵𝘪𝘰𝘯𝘴上。广西大学为该论文的第一完成单位,胡丹丹与硕士毕业生李轩为共同第一作者,宋星桔为通讯作者。

弓形虫病是由弓形虫寄生引起的一种重要人兽共患病,其生命周期极为复杂,有多种发育阶段,能够在人和猫等不同宿主中进行“身份”切换(比如致病的速殖子、潜伏的缓殖子),还会切换分裂方式(速殖子1分2,裂殖子1分N)。在之前的研究中只知道有个“抑制器”(MORC复合体)能关掉不该有的“身份基因”,但一直不清楚谁是“激活器”——负责打开速殖子自身必需的基因,维持它的正常身份和分裂。调控其不同阶段分裂方式转换的核心机制尚不明确,这也是该领域研究的瓶颈问题。
针对这一难题,研究团队取得了三个核心新进展:
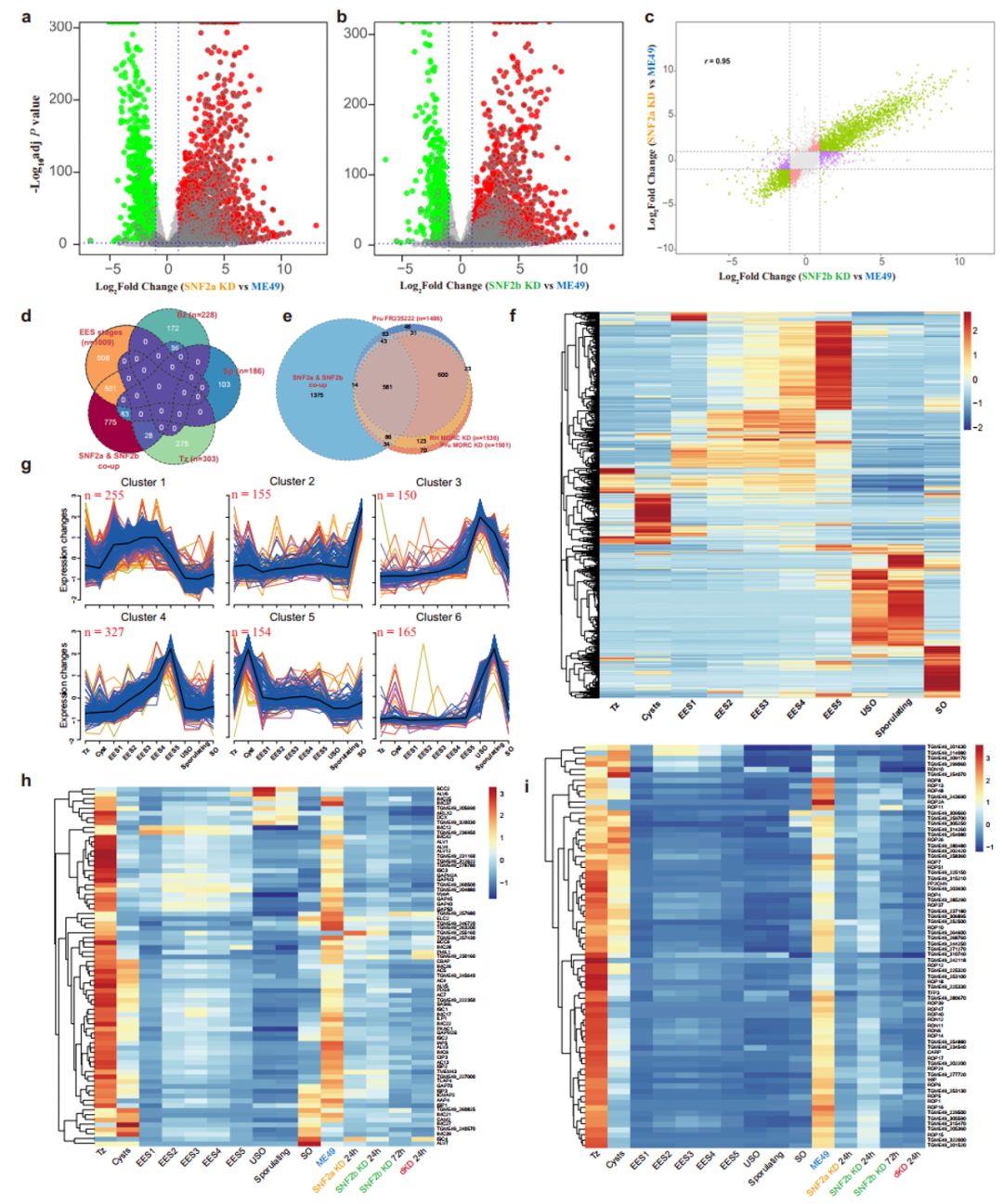
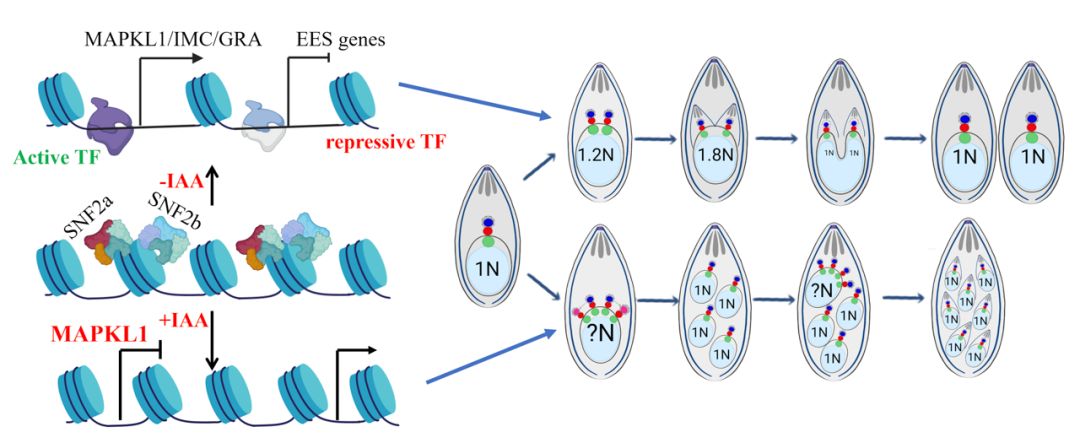
找到了“激活器”。首次揭示SWI/SNF染色质重塑复合体是维持弓形虫速殖子分裂方式所必需的核心激活因子。两个复合体的核心亚基SNF2a和SNF2b是弓形虫速殖子阶段生长所必需的。当复合体功能缺失时,寄生虫的分裂模式会从有序的“一分为二”向混乱的“一分为多”发生转变,并错误地启动了本应被抑制的其他发育阶段的转录程序。SWI/SNF复合体作为染色质重塑因子,通过维持速殖子关键基因转录起始区域的染色质开放性来确保其正常表达,并与已知的抑制因子MORC复合体协同作用,实现了对基因表达的双重调控,从而确保寄生虫基因表达和分裂过程的准确性。
揭秘“身份维稳”功能。如果没有SWI/SNF复合体,速殖子会“身份错乱”——本该1分2的分裂变成1分N的异常模式,还会长出多个细胞核、积累不该有的淀粉颗粒,最后走向死亡。
弄清分子机制。SWI/SNF会主动“打开”速殖子自身基因的开关(让染色质变开放),同时还会和“抑制器”MORC合作,一起关掉裂殖子的基因,双重保障速殖子不“串味”。
此次研究的突破意义重大,不仅首次明确了SWI/SNF复合体在弓形虫里的作用,解释了寄生虫“身份切换”和分裂调控的核心机制,而且提供了新药物靶点,这个复合体对弓形虫生存至关重要,且和人类体内的同类复合体不一样,能针对性开发新药,为治疗弓形虫病提供了全新思路。
据悉,该团队一直致力于人兽共患弓形虫病和畜禽球虫病的分子生物学、药物作用机制和耐药机制等研究。近年来,团队聚焦寄生虫表观遗传调控这一前沿热点,先后解析了多个转录因子和染色质重塑复合物对虫体生长发育的调控作用。一系列原创性成果发表在𝘕𝘢𝘵𝘶𝘳𝘦 𝘊𝘰𝘮𝘮𝘶𝘯𝘪𝘤𝘢𝘵𝘪𝘰𝘯𝘴、𝘮𝘉𝘪𝘰、𝘝𝘦𝘵𝘦𝘳𝘪𝘯𝘢𝘳𝘺 𝘙𝘦𝘴𝘦𝘢𝘳𝘤𝘩等国内外期刊上。
